Bariumtitanat
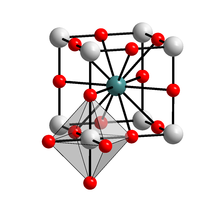
| Kristallstruktur | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||
| _ Ba2+ _ Ti4+ _ O2− | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Bariumtitanat | ||||||||||||||||||
| Andere Namen |
Bariumtitanat(IV) | ||||||||||||||||||
| Verhältnisformel | BaTiO3 | ||||||||||||||||||
| Kurzbeschreibung |
weißes bis graues, geruchloses Pulver[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 233,19 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
5,85 g·cm−3[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit |
nahezu unlöslich in Wasser[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| MAK |
0,5 mg·m−3 Barium[1] | ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Bariumtitanat ist ein Mischoxid von Barium und Titan aus der Gruppe der Titanate und kristallisiert in der Perowskit-Struktur.
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]BaTiO3 kann nach der klassischen Mischoxid-Methode aus BaCO3 (Bariumcarbonat) und TiO2 (Titandioxid) in einer Festkörperreaktion, dem sogenannten Kalzinieren, bei einer Temperatur von 1200 °C hergestellt werden.
Moderatere Bedingungen bietet die Kristallisation aus schmelzflüssiger Lösung. Stöchiometrische Mengen Bariumcarbonat und Titandioxid (Anatas) werden mit einem großen Überschuss Natriumchlorid vermengt oder mit Kaliumfluorid überschichtet. Im Ofen kristallisiert bei 1000 bis 1160 °C das Bariumtitanat aus. Nach Auswaschen der Salzreste erhält man es in sehr reiner Form, in feinen Kristallen.[4]
Wird die Reaktion in einem Platintiegel in einer Schmelze aus Kaliumfluorid bei 1160 °C unter Verwendung von käuflichem gepulverten Bariumtitanat vorgenommen, so erhält man ausgeprägte Einkristalle der Verbindung, die mitunter verzwillingt vorliegen.[4]
Physikalische Eigenschaften
[Bearbeiten | Quelltext bearbeiten]
Bariumtitanat gehört zur Gruppe der Elektrokeramiken. Bariumtitanat ist ein Ferroelektrikum und besitzt eine ausgeprägte Hystereseschleife. Wie alle Ferroelektrika besitzt es eine hohe Permittivität, welche stark von der elektrischen Feldstärke abhängt.
Bariumtitanat kristallisiert in zwei polymorphen Gittertypen, dem hexagonalen Gittertyp und der Perowskit-Struktur. Bei Temperaturen unter 120 °C liegt es als tetragonal verzerrte Modifikation der Perowskit-Struktur mit den Gitterkonstanten a = 399,2 pm und c = 403,6 pm vor[4], bei der das Titanion gegenüber den Sauerstoffionen in z-Richtung verschoben ist. Daraus resultieren ein Dipolmoment der Elementarzelle und die Polarisation. Bei Erreichen der Curie-Temperatur von 120 °C erfolgt die Phasenumwandlung zur kubischen Perowskit-Struktur[4], bei der sich das Titanion genau im Zentrum des Oktaeders aus Sauerstoffionen befindet. Damit hat die Elementarzelle des Kristalls kein Dipolmoment mehr und der Kristall ist nicht mehr ferroelektrisch. Bei hohen Temperaturen erfolgt die Phasenumwandlung in die hexagonale Phase. Diese Phasenumwandlung erfordert eine umfangreichere Umordnung der Ionen als der Übergang bei 120 °C. Bei größeren Kristallen kommt es deshalb häufig vor, dass sie bei dieser Umwandlung zerbrechen.
Unterhalb von 0 °C liegt eine orthorhombische Symmetrie vor, während sich diese unterhalb von −90 °C in eine trigonale umwandelt.[4]
Verwendung
[Bearbeiten | Quelltext bearbeiten]Aufgrund der ferroelektrischen, dielektrischen und pyroelektrischen Eigenschaften werden Bariumtitanat sowie verwandte Perowskite wie Pb(Zr,Ti)O3 unter anderem in der Elektronik und Sensorik als Werkstoff verwendet. Beispiele sind Kaltleiter sowie die Verwendung als nichtlineares Dielektrikum in hochkapazitiven Keramikkondensatoren. Allerdings ist der konkrete Kapazitätswert stark schwankend und unter anderem von der an dem Kondensator angelegten Spannung und der Temperatur abhängig.
Literatur
[Bearbeiten | Quelltext bearbeiten]- Arthur R. von Hippel: Ferroelectricity, Domain Structure, and Phase Transitions of Barium Titanate. In: Rev. Mod. Phys. 1950, 22, S. 221–237, doi:10.1103/RevModPhys.22.221.
Weblinks
[Bearbeiten | Quelltext bearbeiten]Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e Datenblatt Bariumtitanat bei Alfa Aesar, abgerufen am 7. Januar 2010 (Seite nicht mehr abrufbar).
- ↑ a b Eintrag zu Bariumtitanat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2021. (JavaScript erforderlich)
- ↑ Nicht explizit in Verordnung (EG) Nr. 1272/2008 (CLP) gelistet, fällt aber mit der angegebenen Kennzeichnung unter den Gruppeneintrag barium salts, with the exception of barium sulphate, salts of 1-azo-2-hydroxynaphthalenyl aryl sulphonic acid, and of salts specified elsewhere in this Annex im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ a b c d e Francis S. Galasso: Barium titanate, BaTiO3 (Barium titanium(IV) oxide). In: Aaron Wold and John K. Ruff (Hrsg.): Inorganic Syntheses. Band 14. McGraw-Hill Book Company, Inc., 1973, ISBN 07-071320-0 (defekt), S. 142–143 (englisch).

